Für das Verfahren A ist die Teilgleichung zu Mangan tabelliert.
die Teilgleichung für Oxalat ist: C2O42-
die Aufstellung der Gesamtgleichung damit ist eigene (einfache) Übungsaufgabe!
|
letzte Beispiele |
REDOXGLEICHUNGEN - X. Letzte Beispiele
Permanganat oxidiert in saurer Lösung
Oxalat-Ionen zu CO2; Mn(II) entsteht .
Für
das Verfahren A ist die Teilgleichung zu Mangan tabelliert.
die Teilgleichung
für Oxalat ist: C2O42- ![]() 2 CO2 + 2 e-
2 CO2 + 2 e-
die Aufstellung der Gesamtgleichung damit
ist eigene (einfache) Übungsaufgabe!
Für den 1. Schritt mit den Redoxzahlen setzen wir sofort ein, dass 1
Oxalat 2 CO2 liefern musss: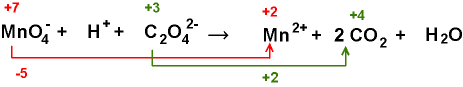
Damit
ist die Änderung der Ox.-Zahlen auch +2 (zweimal von +3 auf +4).
Abgleich
der Änderung der Ox.-Zahlen: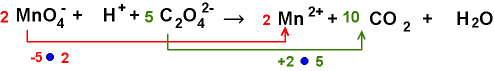
Abgleich
des O: 8 O aus 2 Permanganat erfordern 16 H+ und liefern 8 H2O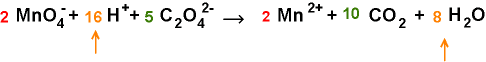
Kontrolle
der Ladungs-Bilanz: links (-2,+16,-10) = +4; rechts: +4
Fazit: Auch dieses Problem ist lösbar, aber Übung
ist nötig!
Entwicklung der Teilgleichung zu Oxalat
(diese ist nicht tabelliert)
C2O42-
![]() 2 CO2 ; es wird sofort die richtige Anzahl von C Atomen berücksichtigt.
2 CO2 ; es wird sofort die richtige Anzahl von C Atomen berücksichtigt.
Die
Oxidationszahl der C-Atome ändert sich von +3 auf +4; weil 2 C vorhanden
sind
werden in dieser Oxidation 2 Elektronen abgegeben: C2O42-
![]() 2 CO2 + 2 e-
2 CO2 + 2 e-
Disproportionierungsreaktion
Ein Stoff
wird reduziert und oxidiert - und zwar durch sich selbst. Der Stoff ist
demnach
Oxidations- und Reduktionsmittel; die Ox.-Zahl erhöht
und erniedrigt sich.
Chlor bildet in Wasser (teilweise) HCl und HClO.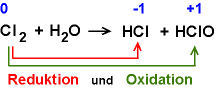
HClO zerfällt (teilweise) in HCl und HClO3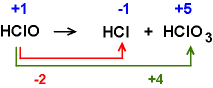
und
nach dem Abgleich (Erhöhung: Erniedrigung = 2:1)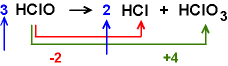
WEITER: ... und nun ... Alles Weitere ist Übung !