(1) H2O2 + 2H+ + 2 e-
(2) 2 I-
Der Abgleich ist schon vorhanden, beide Gleichungen müssen nur addiert werden.
H2O2 + 2 H+ + 2 I-
Wenn die Teilgleichungen vorhanden (tabelliert) sind, ist dieser Weg sehr einfach.
|
2. Beispiel |
REDOXGLEICHUNGEN - VIII. REDOXGLEICHUNGEN - Zweites Beispiel
Wasserstoffperoxid oxidiert in saurer Lösung Iodid zu Iod.
Verfahren A - Teilgleichungen
Tabelliert sind
(1)
H2O2
+ 2H+ + 2 e- ![]() 2 H2O
2 H2O
(2) 2 I-
![]() I2 + 2e-
I2 + 2e-
Der Abgleich ist schon vorhanden,
beide Gleichungen müssen nur addiert werden.
H2O2
+ 2 H+ + 2 I- ![]() 2 H2O + I2
bzw.
H2O2
+ 2 HI
2 H2O + I2
bzw.
H2O2
+ 2 HI ![]() 2 H2O + I2
2 H2O + I2
Wenn die Teilgleichungen vorhanden (tabelliert) sind, ist
dieser Weg sehr einfach.
Verfahren B - Abgleich der Oxidationszahlen
Das Verfahren ist hier etwas komplizierter, weil nicht sofort
klar ist, wie die Angabe "in saurer Lösung"
berücksichtigt
werden muss. Die hier benutzte Überlegung ist immer dann wichtig, wenn
auf beiden Seiten
der Gleichung verschieden viele Sauerstoff- oder Wasserstoff-Atome
auftreten!
Der scheinbar richtige Ansatz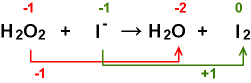
zeigt,
dass von den Atomsorten O und I verschieden viele Atome auf beiden Seiten vorliegen.
Besser
wäre also: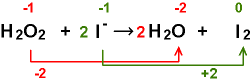
Jetzt
stimmt die Anzahl von O und I.
Falsch sind noch 2 Dinge: 1. links 2 H und
rechts 4 H; 2. links die Ladung -2 und rechts 0.
Durch Hinzufügen von
2 H+ auf der linken Seite stimmen sowohl die Anzahl H und die Ladung: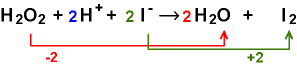
Fazit:
Das Problem ist lösbar, aber Übung ist nötig!
WEITER: Der "H+ - Trick"