![]()
|
"H+-Trick" |
|
|
|
|
|
|---|
|
Übersicht |
REDOXGLEICHUNGEN - IX. Der "H+-Trick"
Das bei der vorigen Redoxgleichung mit H2O2 schon benutzte Verfahren ist:
Alternativ kann man zuerst mit so vielen H+ ergänzen, dass
die Ladungsbilanz erfüllt
ist und dann die Bilanz der Atomsorten als
Kontrolle durchführen.
Permanganat oxidiert in saurer Lösung
Fe(II)- zu Fe(III)-Ionen; Mn(II) entsteht .
Für
das Verfahren A sind die Teilgleichungen tabelliert.
die Aufstellung der
Gesamtgleichung damit ist eigene (einfache) Übungsaufgabe!
|
... ich will trotzdem die Lösung sehen! |
Verfahren B
Auf den ersten Blick sieht man, dass wegen MnO4- auf
der linken Seite dort auch H+
vorkommen muss und entsprechend
viele H2O rechts zum Ausgleich von O nötig sind.
1. Schritt:
Anpassung über Redoxzahlen
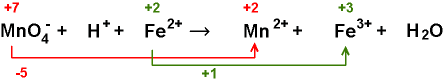
nach
Ausgleich: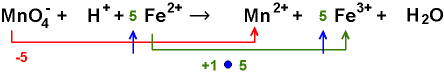
Das
Verhältnis Mn zu Fe ist damit richtig.
2. Schritt: Kompletter
Abgleich - beginnend mit der Atomsorten-Bilanz:
4 O links erfordern 4 H2O
rechts und als Folge davon erfordern nun 8 H rechts auch 8 H links:
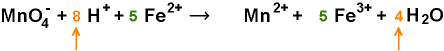
Kontrolle
der Ladungen: links (-1,+8,+10) = +17; rechts (+2,+15) = +17;
die Reaktionsgleichung
ist völlig abgeglichen (Atomsorten- und Ladungs-Bilanz).
Alternativer
2. Schritt: Abgleich beginnend mit der Ladungs-Bilanz:
links (-1,+1,+10)
= +10; rechts (+2,+15) = +17; d.h. links fehlen noch +7 Ladungen.
Nach Hinzufügen
von 7 H+ sind links 8 H+ vorhanden, rechts müssen
4 H2O für diese
8 H+ dazukommen; Kontrolle: die
4 O kommen aus MnO4- und die Reaktionsgleichung
ist
wieder völlig abgeglichen.
Fazit: Auch dieses Problem ist lösbar, aber Übung
ist nötig!
WIE GEHT MAN VOR, WENN MAN SELBST DIE TEILGLEICHUNGEN
AUFSTELLEN MUSS?
Wir werden sehen, dass ähnliche
Überlegungen wie oben beim Gesamtverfahren eine Stufe
vorher bei den
Teilgleichungen nötig sind.
REZEPT:.
1. Schreibe das Redoxpaar mit Oxidationszahlen!
2. Gleiche
die Änderung der Oxidationszahlen mit Elektronen aus!
3. Gleiche die
Ladungsbilanz aus durch Zufügen von H+ (oder OH-)!
--- etwas mehr dazu! ![]()
4.
Gleiche die Massenbilanz durch Hinzufügen von H2O aus!
Fe2+ ![]() Fe3+; dies ist eine Oxidation (also Elektronenabgabe)
Fe3+; dies ist eine Oxidation (also Elektronenabgabe)
Wir
gleichen die Zunahme der Ox.-Zahl um 1 durch 1 e- aus: Fe2+
![]() Fe3+ +
e-
Fe3+ +
e-
Die Ladungs- und die Massenbilanz sind erfüllt, die
Teilgleichung ist fertig.
MnO4- ![]() Mn2+ (in saurer Lösung); eine Reduktion (also Elektronenaufnahme)
Mn2+ (in saurer Lösung); eine Reduktion (also Elektronenaufnahme)
Die
Ox.-Zahl des Mangans nimmt von +7 auf +2 ab; Ausgleich durch 5 e-:
MnO4-
+ 5 e- ![]() Mn2+ ; die Ladungsbilanz - links -6, rechts +2 - muss durch
Mn2+ ; die Ladungsbilanz - links -6, rechts +2 - muss durch
Zugabe
von 8 H+ korrigiert werden. (dann ist die Ladung auf beiden Seiten
+2)
MnO4- + 5 e- +
8 H+ ![]() Mn2+ .
Mn2+ .
Die Massenbilanz von H und O wird durch Zugabe
von 4 H2O richtig gestellt:
MnO4- +
5 e- + 8 H+ ![]() Mn2+ + 4 H2O
Mn2+ + 4 H2O
Kontrolle zeigt: Ladungs-
und Massenbilanz stimmen.
WEITER: letzte Beispiele