CuCl2 + Al
|
1. Beispiel |
REDOXGLEICHUNGEN - VII. REDOXGLEICHUNGEN - Erstes Beispiel
Kupfer(II)chlorid reagiert zu Kupfer und oxidiert dabei Aluminium zu Aluminiumchlorid.
1. Schritt: Reaktionsgleichung - Angabe
der vorkommenden Stoffe
CuCl2
+ Al ![]() Cu
+ AlCl3
Cu
+ AlCl3
2. Schritt: Reaktionsgleichung - Isolieren
des "relevanten" Teils
Nur die Ox.-Zahlen
von Cu und Al ändern sich, die Ox.-Zahl von Cl bleibt gleich.
Das Gerüst
für den "relevanten" Teil ist damit:
Cu2+
+ Al ![]() Cu
+ Al3+
Cu
+ Al3+
3. Schritt: Verfahren A
- Teilgleichungen
Tabelliert
sind die beiden Teilgleichungen
(1)
Cu2+ + 2 e-
![]() Cu (Reduktion)
Cu (Reduktion)
(2) Al ![]() Al3+ + 3e- (Oxidation)
Al3+ + 3e- (Oxidation)
Die
Anzahl aufgenommenener und abgegebener Elektronen muss gleich sein.
Gleichung
(1) wird mit 3 und Gleichung (2) mit 2 multipliziert.
(1') 3 Cu2+ + 6 e-
![]() 3 Cu
3 Cu
(2') 2 Al ![]() 2 Al3+ + 6 e-
2 Al3+ + 6 e-
Bei
der Bildung der Summe der beiden Teilgleichung kürzt sich die Anzahl e-.
3
Cu2+ + 2 Al ![]() 3 Cu + 2 Al3+
3 Cu + 2 Al3+
Durch
Hinzufügen von 6 Cl auf beiden Seiten folgt die Endgleichung
3
CuCl2 + 2 Al ![]() 3 Cu + 2 AlCl3
3 Cu + 2 AlCl3
3. Schritt: Verfahren B - Abgleich der Oxidationszahlen
Die Oxidationszahlen der "relevanten" Stoffe und
deren Änderungen werden festgestellt.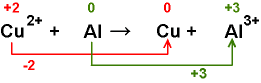
Die
Oxidationszahl von Cu nimmt um 2 ab, die Oxidationszahl von Al um 3 zu.
Die Änderungen werden abgeglichen, die dabei vorkommenen
Faktoren liefern die stöchiometrischen Koeffizienten.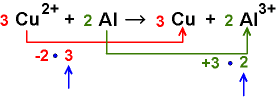
Bei
Cu wird mit 3 multipliziert, bei Al mit 2. Insgesamt ist so die Summe der Ab-
und Zunahme der Ox.-Zahlen 0!
Nach Hinzufügen von 6 Cl auf beiden Seiten
folgt dieselbe Endgleichung wie bei Verfahren A.
WEITER: Zweites Beispiel